


Por: Ma. Celeste Olivero Médica Veterinaria MP: 637
¿CÓMO DEFINIMOS DOLOR?
Es definido por la Asociación Internacional para el Estudio del Dolor como “una experiencia emocional desagradable, asociada con un daño tisular real o potencial, o descripto en los términos de dicho daño”. Esta definición enfatiza la importancia de la comunicación verbal en la evaluación del dolor humano, un aspecto que por supuesto no puede ser satisfecho en la evaluación del dolor animal. Justamente por este motivo, frecuentemente es subestimada la capacidad de los animales de experimentar dolor, aún a pesar de que la evidencia científica demuestra que existe un fuerte paralelismo en la respuesta fisiológica de humanos y animales a un estímulo nociceptivo (Gallo M., 2010).
Para comenzar a hablar de la idea de instaurar terapias “Multimodales” de analgesia, primero debemos saber en que consiste, como es su fisiopatología y en que receptores vamos a trabajar a la hora de instaurar una estrategia analgésica.
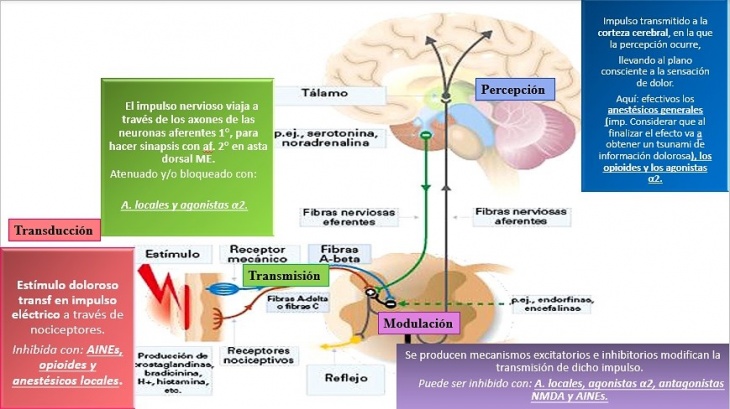
La vía del dolor o nocicepción consiste en 4 pasos: Transducción, Transmisión, Modulación y Percepción.
Transducción: Primer paso en el cual una noxa genera liberación de mediadores inflamatorios (como lo son las prostaglandinas) a partir de tejidos dañados. Estos mediadores proinflamatorios, son a su vez transformados en energía eléctrica por los nociceptores. A este nivel, la vía del dolor puede ser inhibida a través del uso de antiinflamatorios no esteroidales, opioides y anestésicos locales.
Transmisión: el impulso nervioso viaja a través de los nervios periféricos a la médula espinal, proceso que puede ser atenuado y/o bloqueado con el empleo de anestésicos locales y agonistas alfa 2. En el asta dorsal de la médula espinal, el dolor es modulado y puede ser inhibido con el uso de anestésicos locales, agonistas alfa 2, antagonistas de los receptores N-Metil-D-Aspartato (NMDA) y Antiinflamatorios No Esteroidales (AINEs).
Modulación: ocurre a nivel de médula espinal donde se produce liberación de sustancias endógenas que, como dice su nombre, intentan “modular” la transmisión de dolor que se dirige hacia la corteza cerebral, donde la sensación de dolor será llevada al plano consciente. Aquí son efectivos agonistas alfa 2, anestésicos locales, Antagonistas NMDA y AINES.
Y por último, el proceso de Percepción, ocurre a nivel de la corteza cerebral, y aquí son efectivos: opioides y los agonistas alfa 2.

¿POR QUÉ INSTAURAR MÉTODOS MULTIMODALES?
En la actualidad, las recomendaciones médicas-farmacológicas para el manejo del dolor incluyen dos aproximaciones: el enfoque preventivo y el multimodal.
El enfoque preventivo contempla la administración de analgésicos antes de un estímulo doloroso, lo que minimizaría los efectos de la sensibilización central y periférica, redundando en una disminución de la intensidad y duración del dolor postoperatorio, como también disminuye las posibilidades de que se establezca el dolor crónico.
Mientras que el enfoque multimodal implica la selección de drogas analgésicas de diferentes clases que afectan distintas porciones de las vías del dolor, resultando en un efecto sinérgico que optimiza la analgesia al tiempo que minimiza los efectos colaterales de las drogas.
Las drogas más frecuente empleadas en protocolos de analgesia multimodal incluyen opioides, AINEs, anestésicos locales, antagonistas NMDA y agonistas alfa 2.
La elección de las drogas empleadas para tratar el dolor dependerá de la causa subyacente del mismo, de su severidad y duración, pero también de la edad del animal y de su estado de salud en general. A modo de ejemplo, cuando se compara el uso de drogas en animales muy jóvenes (cachorros de menos de 3 meses de vida) y animales gerontes (superando el 75% de su expectativa de vida) es necesario considerar que las diferencias en el perfil farmacocinético en cada caso, determinarán cambios en la dosificación e intervalo de administración.
Finalmente, el intervalo entre dosis se ve influenciado también por la severidad del dolor, factores del paciente y la combinación de drogas empleadas, por lo que debería en general ser ajustado de acuerdo con la respuesta del paciente.
Teniendo en cuenta todo lo anteriormente expuesto, es que se considera necesaria la sistematización de la información disponible en la literatura científica sobre protocolos de analgesia multimodal, con la finalidad de analizar en forma crítica las distintas posibilidades de abordaje que presenta esta estrategia de prevención o tratamiento del dolor en pequeños animales, en las situaciones que con mayor frecuencia se presentan en la práctica clínica y quirúrgica en Medicina Veterinaria.
PREVENCION VS. TRATAMIENTO
Debemos tener en cuanta cuales son nuestros objetivos en cada estrategia analgésica, cuando queremos prevenir un dolor, por ejemplo, el quirúrgico nuestra meta es prevenir la estimulación de los receptores que actúan en la generación del dolor, es decir la sensibilización periférica. Y al tratar un dolor ya instaurado, donde el paso antes mencionado ya se ha producido nuestro objetivo cambia, y en este caso, será prevenir que esa algesia se haga crónica, conocida como, sensibilización central. Si esto no se previene, el animal tendrá hiperalgesia, alodinia debido a la estimulación prolongada de sus receptores, presentando dolor frente a estímulos normalmente no dolorosos.
¿CON QUE HERRAMIENTAS CONTAMOS?
Entre los más usados podemos mencionar:
- AINES
- OPIOIDES
- ANESTÉSICOS LOCALES
- AGONISTAS α2
- ANTAGONISTAS NMDA

ANTINFLAMATORIOS NO ESTEROIDALES
Este tipo de fármacos actúa a nivel de la transducción, modulación y percepción.
Acción: (-) de la ciclooxigenasa (COX). Latencia: 15 – 60min. Unión a proteínas plasmáticas (98-99%): Precaución en pacientes con hipoproteinemia.
Uso crónico: valorar toxicidad, c/ 15 ds.
Además, poseen efecto ANTIONCOGÉNICO: En tumores que descaman células. Como osteosarcomas, Carcinomas, melanomas, etc. Inhiben la angiogénesis y crecimiento tumoral.
Entre los más usados se encuentran los específicos de COX 2, como el Meloficam, Firocoxib, etc.
Meloxicam: comúnmente usado en dosis de 0,1 – 0,2 mg/kg c/24hs. En uso crónico: Primeras 72hs: Dosis completa, posteriormente: 75% de la dosis antinflamatoria es la analgésica, por lo que podemos usar 0,07mg/kg.
Firocoxib: 5 mg/kg c/24hs Oral. (Caninos).
DIPIRONA/ METAMIZOL
Efecto analgésico sobre prostaglandinas sintetasas a nivel de SNC. Inhibe las fibras Delta intermediarias en la transmisión del dolor. Muy útil en analgesia visceral, y de elección para instaurar una terapia en felinos. Podemos combinarlo con AINES o AIES. Dosis recomendadas (sujetas a cambios según estado del paciente): Para Caninos: 20-25mg/kg - Felinos: 10-15mg/kg. En Infusiones a ritmo constante: 10mg/kg/hs.
OPIOIDES
Eficientes en 3 niveles de las vías del dolor, desde la transducción, modulación hasta la percepción a nivel central.
Se dividen en 3 grupos:
- Agonistas µ puros.
- Agonistas-antagonistas
- Antagonistas puros.
La analgesia en mamíferos está dada principalmente por receptores µ. Y en aves, tenemos por receptores K.
Por lo que nuestros objetivos al interactuar con receptores opiáceos en mamíferos será utilizar fármacos agostas µ puros.
AGONISTAS µ PUROS
Brindan analgesia supraespinal. Causan también sedación depresión respiratoria y disminución de la FC. A nivel de la presión arterial: no reflejan cambios significativos, excepto la morfina, que causa hipotensión, por liberación de histamina. Pacientes cardiópatas: mantiene VMC adecuado. A nivel de sistema gastrointestinal: Vómitos por estimulación de receptores en Centro emético, Ojo en pacientes sospecha de Cuerpo extraño.
Entre los más usados podemos mencionar de menor a mayor potencia sobre los receptores μ:
Morfina
Fentanilo: Acción corta (Efecto dura aprox. 30 minutos). Debido a su corta vida media, se recomienda su uso intrahospitalario en infusión continua. Dosis aproximadas: bolo: 2-5mcg/kg IV + CRI: de 5-10mcg/kg/hs. Considerar: redistribución al tejido graso, en infusiones superior a 2 hs, satura tej adiposo y prolonga su efecto hipnótico.
Remifentanilo: De acción Ultracorta (3-4minutos). Depresión cardio respiratoria dosis dependiente. Escasa redistribución en tejidos periféricos. Metabolizado por esterasas plasmáticas, por lo que es de elección en pacientes con afección hepatorenal. Y también por el tamaño de su partícula y el poco paso por la placenta es de elección en cesáreas, ya que los cachorros de este modo nacen con total vitalidad. Su utilización es exclusivamente en CRI. En dosis de: 0,1 - 1 mcg/kg/min.
AGONISTAS PARCIALES Y AGONISTAS-ANTAGONISTAS
Butorfanol: Agonista antagonista, con baja activ en rc μ, agonista κ y sigma.
Nalbufina: Agonista rc. Kappa – Antagonista μ.
No brindan analgesia eficiente en procedimientos cruentos, en mamíferos, por su antagonismo en receptores μ. Útiles para realizar sedación, o combinados, en neuroleptoanalgesia para procedimientos menores.
TRAMADOL
Agonista μ sintéticos débil de escasa potencia.
“Analgésico adyuvante - Antihiperalgésico”
Inhibe la recaptación de serotonina y noradrenalina.
Debe ser metabolizado para tener acción opioide, metabolito: O-desmetil tramadol (M1), diferente biodisponibilidad, en caninos y felinos, luego de una dosis oral, donde se obtiene un 60% en perros, y un 100% en felinos.
En un estudio reciente, donde se evaluó la vida media del Metabolito activo (M1) en caninos y felinos. Se comprobó que en los primeros, el M1 tenía una vida media de 1.6hs, por lo que no obtenemos un beneficio de analgesia prolongada, si no que podemos utilizarlo para evitar la sensibilización central. No así en gatos, donde su metabolito duraba hasta 4-6 horas.
Y por último, un concepto importante, al ser un fármaco “adyuvante” y de baja potencia siempre debe utilizarse en combinación con otras drogas.


ANESTESICOS LOCALES
Bloquean origen y propagación del impulso nociceptivo.
Los más usados en Argentina: Lidocaína, Bupivacaina.
- Lidocaína: es utilizada de forma lenta endovenosa, en bolo y en infusión continua, a dosis de 0.6mg/kg.
- Bupivacaina: es muy útil en dolor de tipo visceral, ya que nos dará analgesia de 4-6hs, en forma intraperitoneal a dosis de 1mg/kg.
AGONISTAS α 2:
Estimulación de receptores α 2 ubicados en el SNC.
(Ej: Xilazina y dexmedetomidina)
Consideraciones: Tienen efecto analgésico equipotente a la morfina. Opioides y alfa 2 agonistas: SUMAN, ya que donde hay receptores opioides hay rc alfa 2.
Desventajas: Arritmias, hipotensión, depresión respiratoria (dosis dependiente) – Inhibe liberación insulina – precaución: pacientes con diabetes y contraindicado en: menores 12 semanas, y en pacientes con cardiomiopatías: donde el VMC depende de la FC, ya que éstos producen bradicardia, y con ello una disminución del VMC.
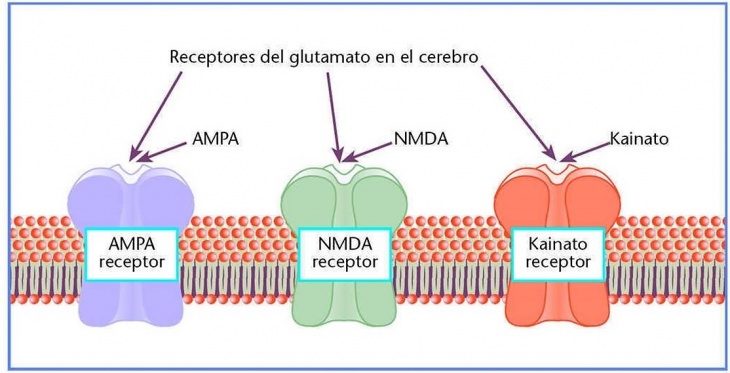
ANTAGONISTAS NMDA
(NMDA: Rc que participan en la liberación de glutamato)
KETAMINA:
Única dosis aporta 30 minutos de analgesia. P/ prolongar efecto, se realiza infusión continua.
Previa dosis carga de 0,6 - 1 mg/kg IV + infusión continua a 0,6mg/kg/hs.
BLOQUEANTE DE RECEPTORES NK1
Entre ellos se encuentra el Maropitant, siendo de los recomendados en analgesia visceral, concomitantemente con el metamizol.
Dosis recomendada: 0,5 – 1 mg/kg. (Fel – Caninos)
CRI: 30mcg/kg/hs (hasta por 24 hs).
Con este breve artículo podemos ver que tenemos muchas herramientas en el consultorio para manejar el dolor de manera eficiente, completo y con los efectos secundarios indeseables disminuidos.
Actualmente se considera el Dolor como una enfermedad más, siendo este muy importante a la hora de actuar sobre nuestros pacientes, es una responsabilidad ética y profesional, hagamos que nuestros pacientes no sientan dolores post operatorios, evitemos el dolor intra y post quirúrgico desde la medicación preanestésica, o incluso desde el día anterior si es posible.
Hagamos que aquellos que llegan con dolor a la clínica, puedan cálmarlo. Y quienes padecen dolor crónico puedan ser acompañados para tener una mejor calidad de vida.


Por último, no olvidemos…






